اپروچ به دیسپلازی رشدی (مادرزادی) لگن (DDH)
دیسپلازی رشدی لگن (DDH) طیفی از شرایط مربوط به رشد لگن را در نوزادان و کودکان خردسال توصیف می کند. این شامل رشد غیر طبیعی استابولوم و پروگزیمال فمور و بی ثباتی مکانیکی مفصل ران می باشد. نوزادان اغلب در چند هفته اول زندگی دچار شلی فیزیولوژیک مفصل ران و عدم بلوغ استابولوم می شوند. در بیشتر موارد، شلی برطرف می شود و استابولوم به طور طبیعی رشد می کند. با ارزیابی عوامل خطر، معاینه فیزیکی سریال باسن و استفاده مناسب از تصویربرداری، اکثر کودکان مبتلا به لگن پاتولوژیک را می توان به درستی تشخیص داد و بدون عواقب طولانی مدت درمان کرد.
DDH معمولی که معموgh در نوزادان سالم رخ می دهد، تمرکز این بررسی موضوع خواهد بود. دیسپلازی و بی ثباتی هیپ نیز در ارتباط با شرایط دیگر رخ می دهد. دیسپلازی تراتولوژیک هیپ همراه با سندرم های مختلف (به عنوان مثال اهلرز دانلوس، سندرم داون، آرتروگریپوز) و دیسپلازی عصبی عضلانی هیپ زمانی رخ می دهد که در برخی یا همه گروه های عضلانی هیپ ضعف و یا اسپاستیسیته وجود داشته باشد (مثلا در اسپینا بیفیدا یا فلج مغزی). تشخیص و مدیریت دیسپالزی تراتولوژیک و عصبی عضلانی هیپ با تشخیص و مدیریت دیسپلازی هیپ در نوزادان سالم متفاوت است.
اصطلاحات مربوط به مشکلات رشدی لگن
اصطلاحات مربوط به مشکلات رشدی لگن در طول زمان تغییر کرده است. “دیسپالزی رشدی لگن” (DDH) اصطلاح ارجح است.
“رشدی” به “مادرزادی” ترجیح داده می شود، زیرا این بیماری همیشه در بدو تولد وجود ندارد یا قابل شناسایی نیست و در اوایل کودکی ایجاد می شود . “دیسپلازی” به “دررفتگی” ترجیح داده می شود زیرا شامل طیف وسیع تر ی از تغییرات در شکل و موقعیت سر استخوان ران و استابولوم است. “دررفتگی مادرزادی لگن” یک اصطلاح قدیمی است که در زمانی استفاده می شد که اکثر کودکان پس از شروع راه رفتن تشخیص داده می شدند و دررفتگی مادرزادی فرض می شد.
اصطلاحات خاصی که موقعیت، ثبات و شکل لگن را توصیف می کنند در زیر تعریف می شوند:
●Dislocation – از بین رفتن کامل تماس بین سر استخوان ران و استابولوم وجود دارد.
●Subluxation – سر استخوان ران تا حدی خارج از استابولوم است، اما در تماس باقی می ماند.
● Dislocatable – سر استخوان ران در حالت استراحت کاهش می یابد (به عنوان مثال در داخل استابولوم) اما می تواند در موقعیت های دیگر یا با مانورهای معاینه دررفته شود. این لگن با ناپایداری است.
●subluxable/Subluxatable – سر استخوان ران در حالت استراحت کاهش می یابد، اما می تواند با انجام مانورهای معاینه تا حدی دررفته یا سابلوکس شود. این لگن با ناپایداری یا شلی خفیف است.
●Reducible – لگن در حالت استراحت دررفته است، اما سر استخوان ران را می توان با دستکاری (به طور کلی فلکشن و ابداکشن) در داخل استابولوم قرار داد.
●Dysplasia –غیر طبیعی بودن شکل مفصل ران (معمولا کم عمقی استابولوم که حاشیه های فوقانی و قدامی را درگیر می کند)
اپیدمیولوژی
تخمین های بروز DDH کاملا متغیر است و به ابزار تشخیص، سن کودک و معیارهای تشخیصی بستگی دارد. تخمین زده می شود که باسن و لگن قابل جابجایی با دیسپلازی شدید یا پایدار در ۳ تا ۵ کودک از هر ۱۰۰۰ کودک رخ می دهد. از نظر تاریخی، بروز DDH با دررفتگی ۱ تا ۲ در هر ۱۰۰۰ کودک است بی ثباتی خفیف لگن در نوزادان شایع تر است و میزان بروز آن تا ۴۰ درصد گزارش شده است. با این حال، بی ثباتی خفیف و یا دیسپلازی خفیف در دوره نوزادی اغلب بدون درمان برطرف می شود. نوزادان با بی ثباتی خفیف و یا دیسپلازی خفیف در دوره نوزادی نباید در تخمین های بروز لحاظ شوند. گنجاندن آنها منجر به برآورد بیش از حد می شود.
در یک مطالعه آینده نگر، ۹۰۳۰ نوزاد (۱۸۰۶۰ باسن) به طور معمول از نظر DDH توسط معاینه فیزیکی و سونوگرافی در یک تا سه روز زندگی غربالگری شدند. ناهنجاری های سونوگرافی در ۹۹۵ لگن (که نشان دهنده بروز سونوگرافی ۵٫۵ درصد است) تشخیص داده شد. با این حال، در معاینه مکرر در سن دو تا شش هفتگی بدون درمان فواصل، ناهنجاری های باقیمانده فقط در ۹۰ لگن (که نشان دهنده بروز واقعی ۵٫۰ DDH درصد است) شناسایی شد که سپس به درمان ادامه داد. به عبارت دیگر ۹۰ درصد از لگن نوزادان با علائم بالینی یا سونوگرافی DDH قبل از دو تا شش هفتگی به طور خود به خود بهبود یافته است. عقیده ما این است که نوزادانی که دارای یافته های بالینی یا سونوگرافی از شلی خفیف یا دیسپلازی کم هستند، دارای نابالغی طبیعی در رشد لگن هستند و نباید DDH را تشخیص داد یا تحت درمان قرار داد.
عوامل خطر در مشکلات رشدی لگن
DDH در میان نوزادان با عوامل خطر خاص (مانند جنس مونث، وضعیت بریچ در سه ماهه سوم بارداری، سابقه خانوادگی مثبت، قنداق کردن سفت اندام تحتانی) شایعتر است. با این حال به استثنای جنس مونث، اکثر نوزادانی که با DDH تشخیص داده می شوند، هیچ عامل خطری ندارند.
جنسیت زن
خطر DDH در دختران ۹٫۱ درصد برآورد شده است. DDH در نوزادان دختر دو تا سه برابر بیشتر از نوزادان پسر شایع است. در یک متاآنالیز عوامل خطر برای DDH که شامل ۲۴ مطالعه و بیش از ۵۵۶۰۰۰ بیمار بود، نسبت خطر نسبی برای زنان ۵٫۲ (۹۵ %) فاصله اطمینان (CI 2.1-3.1) بود.
افزایش بروز در دختران به افزایش گذرا در شلی رباط مربوط به افزایش حساسیت نوزادان دختر به هورمون ریلکسین مادری نسبت داده شده است. با این حال، برخی از مطالعات این فرضیه را رد می کنند.
افزایش بروز DDH در دختران به سختی قابل جداسازی از افزایش خطر DDH در زایمان بریچ است، که در دختران نیز شایع تر است.
موقعیت بریچ
وضعیت بریچ در سه ماهه سوم بزرگترین عامل خطر برای DDH است. خطر مطلق DDH در دختران بریچ ۱۲ درصد و در پسران بریچ ۶٫۲ درصد برآورد شده است. در یک متاآنالیز عوامل خطر برای DDH که شامل ۱۵ مطالعه (بیش از ۳۵۹۳۰۰ بیمار) بود، خطر نسبی برای تظاهرات بریچ ۸٫۳ (۹۵%) فاصله اطمینان (۲٫۶-۳٫۲ CI) بود. در ادبیات مشخص نیست که آیا مقدار زمانی که در وضعیت بریچ سپری می شود یا نقطه ای در طول بارداری که در آن جنین بریچ بود بر خطر DDH تأثیر می گذارد.
این خطر در نوزادانی که بریچ آزاد دارند (یعنی لگن خمیده، زانو کشیده شده) بیشتر از نمایش بریچ پا است. به نظر می رسد خطر DDH در میان نوزادان بریچ نارس و ترم مشابه است، اگرچه شواهد محدود است. اینکه آیا نسخه خارجی سفالیک موفق بر خطر DDH تأثیر می گذارد یا خیر، در گروهی متشکل از ۴۹۸ نوزاد تک قلو با نمای بریچ در هفته ۳۴ ≥ بارداری که نسخه سفالیک خارجی برای آنها تلاش شد، ارزیابی شد. DDH نیاز به درمان در ۳۵ نوزاد تشخیص داده شد. نسخه سفالیک خارجی موفق با کاهش خطر DDH نیازمند درمان همراه بود (۲٫۸ در مقابل ۹٫۳ درصد؛ نسبت شانس چند متغیره ۲۹٫۰ ۹۵% فاصله اطمینان (۹۵٫۰-۰۹٫۰): CI .) با این حال، مطالعات بیشتری برای روشن شدن رابطه بین نسخه موفق سفالیک و خطر DDH ضروری است. افزایش خطر DDH بدون توجه به روش زایمان وجود دارد. با این حال، کاهش زمان صرف شده در وضعیت بریچ توسط زایمان سزارین قبل از زایمان ممکن است خطر ابتلا به DDH قابل توجه بالینی را کاهش دهد. این در یک بررسی گذشته نگر نشان داده شد که نرخ کاهش DDH را در بین نوزادان بریچ که قبل از شروع زایمان با سزارین زایمان کرده اند نشان داده شد (۳٫۷ درصد در مقابل ۶٫۶ درصد در بین زایمان های سزارین داخل زایمان و ۸٫۱ درصد در بین آنهایی که به صورت واژینال به دنیا آمدند).
سابقه خانوادگی در مشکلات رشدی لگن
به نظر می رسد عوامل ژنتیکی در ایجاد DDH نقش دارند. خطر مطلق DDH در نوزادان با سابقه خانوادگی مثبت تقریباً بین ۱ تا ۴ درصد است. در یک متاآنالیز عوامل خطر برای DDH که شامل چهار مطالعه (بیش از ۱۴۰۰۰ بیمار) بود، خطر نسبی سابقه خانوادگی مثبت ۱٫۳۹ (۹۵ % فاصله اطمینان)۵۷٫۱-۲۳٫۱): CI ) بود. اگر یکی از مجموعه ای از دوقلوها دارای DDH باشد، خطر در دوقلوی دیگر اگر تک تخمکی باشد بیشتر از دو تخمکی است (۴۰ در مقابل ۳ درصد).
در بررسی ۵۸۹ بیمار مبتلا به DDH ،خطر عود در کودکان بعدی زمانی که یک کودک مبتلا وجود داشت، ۶ درصد، زمانی که یکی از والدین مبتلا وجود داشت، ۱۲ درصد و زمانی که یک والدین مبتلا و یک فرزند مبتلا وجود داشت، ۳۶ درصد بود. به نظر می رسد اعضای خانواده کودکان مبتلا به DDH نیز در معرض افزایش خطر دیسپلازی پنهان استابولوم هستند که اغلب قبل از ۳۰ سالگی ایجاد می شود.
قنداق کردن
بروز DDH در جمعیت هایی که از قنداق و تخته گهواره استفاده می کنند افزایش یافته است. این شیوه ها تحرک لگن را محدود می کنند و لگن را در حالت اداکشن و اکستنشن قرار می دهند، که ممکن است در ایجاد DDH نقش داشته باشد. در یک مطالعه تجربی بر روی موش ها، قنداق کردن سنتی در اداکشن و اکستنشن لگن منجر به نرخ دررفتگی و دیسپلازی بیشتر از بدون قنداق کردن شد.
آکادمی اطفال آمریکا (AAP)، انجمن ارتوپدی اطفال آمریکای شمالی (POSNA) و مؤسسه بین المللی دیسپلازی هیپ (IHDI) توصیه می کنند قنداق کردن باسن سالم، که شامل اجازه دادن فضای کافی برای خم شدن مفصل ران و زانو و آزاد کردن حرکت پاها آن است.
سایر شرایط مربوط به مشکلات رشدی لگن
سایر شرایط مربوط به کاهش حرکت جنین یا وضعیت غیرعادی جنین با DDH مرتبط است، اما ثابت نشده است که خطر را افزایش می دهد. اینها عبارتند از تورتیکولی، پلاژیوسفالی، متاتارسوس اضافی، پای پرانتزی، اولین نوزاد بودن، الیگوهیدرآمنیوس، وزن هنگام تولد بیش از ۴ کیلوگرم و حاملگی های چند قلویی.
جنین شناسی و پاتوژنز
رشد طبیعی مفصل ران به تماس طبیعی بین استابولوم و سر استخوان ران بستگی دارد که باعث القای متقابل می شود. رشد غیرطبیعی نتیجه تماس غیرطبیعی است که ممکن است ناشی از عوامل ژنتیکی و محیطی متعدد (داخل رحمی و پس از زایمان) باشد.
در هفته یازدهم بارداری، مفصل ران به طور کامل تشکیل شده است. سر استخوان ران کروی است و عمیقاً در داخل استابولوم قرار گرفته است. با این حال، سر استخوان ران با سرعت بیشتری نسبت به استابولوم رشد می کند، به طوری که در پایان بارداری، سر استخوان ران کمتر از ۵۰ درصد توسط سقف استابولوم پوشانده می شود. در چهار هفته آخر بارداری، لگن در برابر نیروهای مکانیکی، مانند اداکشن که سر استخوان ران را از قسمت مرکزی استابولوم دور میکند، آسیبپذیر است. شرایطی که تحرک جنین را محدود می کند، از جمله موقعیت بریچ، این نیروهای مکانیکی را برجسته می کند. این منجر به تماس خارج از مرکز بین سر استخوان ران و استابولوم می شود.
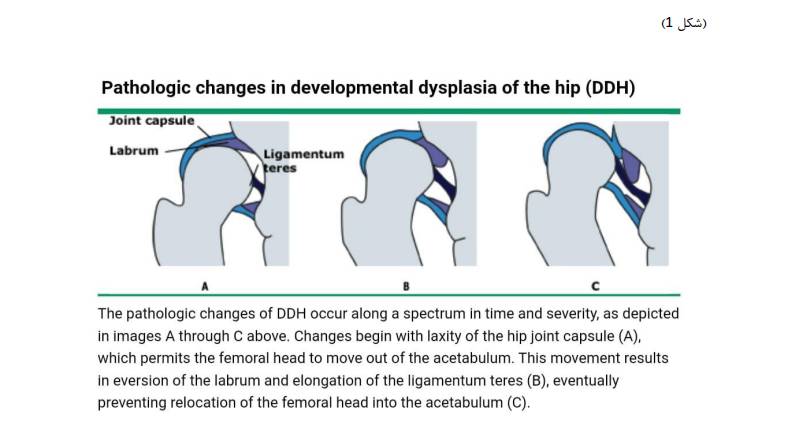
در دوره نوزادی، شلی رباط، لگن در حال رشد را مستعد سایر نیروهای مکانیکی خارجی می کند. قرار گرفتن با باسن کشیده شده (مثال قنداق کردن) می تواند منجر به تماس غیرعادی مفصل ران شود، زیرا سر استخوان ران در داخل یا خارج از استابولوم حرکت می کند. اگر این عوامل ادامه داشته باشند، تماس غیرطبیعی مفصل ران منجر به تغییرات آناتومیک ساختاری می شود. اگر سر استخوان ران عمیقاً در داخل استابولوم قرار نگیرد، لابروم ممکن است به سمت راست و پهن شده و رباط ترز کشیده شود. استخوانی شدن غیر طبیعی استابولوم رخ می دهد و استابولوم کم عمق ایجاد می شود (شکل ۱)
با گذشت زمان، ساختارهای داخل مفصلی هیپرتروفی می شوند، از جمله لابروم با برجستگی ضخیم (نئولیمبوس)، لیگامنتوم ترز، و بافت فیبروچربی (پلوینار). انقباضات در ایلیوپسواس و مجراهای ران ایجاد می شود و کپسول تحتانی به داخل استابولوم خالی کشیده می شود و پتانسیل کاهش بیشتر سر استخوان ران به داخل استابولوم را کاهش می دهد. استابولوم کاذب ممکن است در جایی تشکیل شود که سر استخوان ران با دیواره جانبی لگن بالای استابولوم واقعی تماس پیدا می کند. عدم تماس سر استخوان ران و استابولوم از رشد طبیعی بیشتر مفصل ران جلوگیری می کند.
با یا بدون دررفتگی کامل، لگن ممکن است دچار تغییرات دیسپالستیک شود. معمولا نتیجه یک استابولوم کم عمق با کاهش پوشش قدامی و جانبی سر استخوان ران است. همچنین ممکن است ناسفری سر استخوان ران، زاویه والگوس گردن-شفت، و تداوم آنتورژن اضافی فمورال وجود داشته باشد.
ویژگی های بالینی مشکلات رشدی لگن
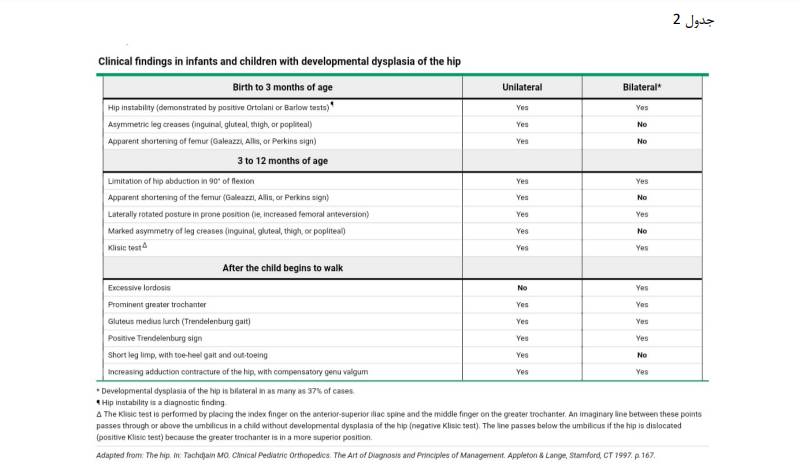
ویژگی های بالینی DDH به سن کودک و شدت ناهنجاری بستگی دارد (جدول ۲)
طیف تظاهرات از بی ثباتی در معاینه نوزاد، تا راه رفتن نامتقارن در کودک نوپا، تا درد ناشی از فعالیت در نوجوانان، تا آرتروز در بزرگسالان متغیر است. هرچه DDH زودتر تشخیص داده شود، درمان ساده تر و موثرتر و نتیجه طولانی مدت بهتری خواهد داشت. شرایطی که با DDH مرتبط است، اما ثابت نشده است که خطر بروز را افزایش می دهند، عبارتند از تورتیکولی، پلاژیوسفالی، متاتارسوس اضافی، پای پرانتزی، نوزاد اول بودن، اولیگوهیدرآمنیوس، وزن هنگام تولد بیش از ۴ کیلوگرم و حاملگی چند قلویی.
نوزادان و کودکان خردسال با دررفتگی لگن درمان نشده به ندرت درد یا محدودیت های دیگری دارند. اکثر کودکان مبتلا شروع به راه رفتن می کنند و در زمان مناسب به نقاط عطف رشد خود می رسند.
معاینه
نمای کلی – ما با دستورالعمل های جامعه حرف های موافقیم که توصیه می کند معاینه DDH در دوره نوزادی شروع شود و در بازدیدهای نظارت بهداشتی تا تقریباً نه ماهگی ادامه یابد و یا کودک به طور مستقل راه برود. معاینه نوزادان و معاینات مطب در سن دو تا چهار هفتگی برای تشخیص زودهنگام DDH اهمیت ویژه ای دارد.
یافته های مربوط به معاینه DDH با توجه به سن متفاوت است (جدول ۲). مهمترین جنبه های معاینه بی ثباتی لگن در نوزاد خردسال و دامنه حرکتی در نوزاد و کودک بزرگتر است. مهم است که معاینه لگن را در حین انجام به والدین توضیح دهید و نتایج را در هر ویزیت مستند کنید.
معاینه کلی — جنبه های مهم معاینه عمومی برای DDH شامل معاینه عصبی و معاینه ستون فقرات و اندام های تحتانی دیستال، جستجوی ناهنجاری های مرتبط با DDH و سایر علل بی ثباتی لگن است.
معاینه عصبی باید شامل ارزیابی حرکت خود به خودی هر چهار اندام و ارزیابی اسپاستیسیتی باشد.
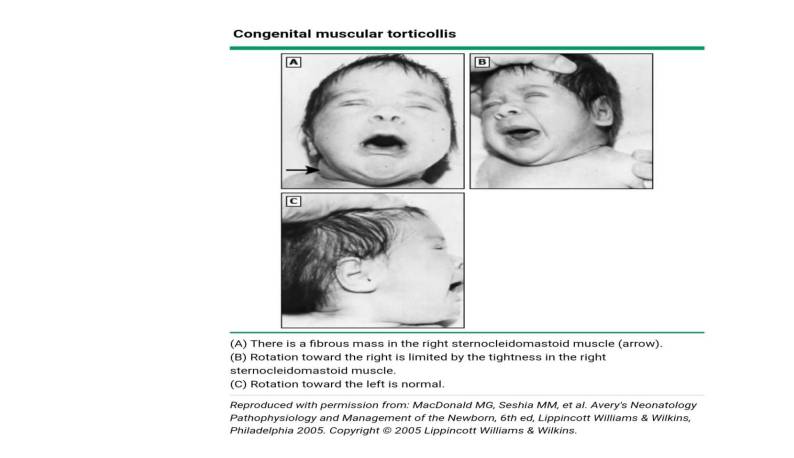
معاینه ستون فقرات باید شامل دامنه حرکتی گردن رحم (به دنبال تورتیکولی (عکس ۱)) تظاهرات پوستی دیس رافیسم ستون فقرات باشد.
یافته های مربوط به سن DDH — یافته های معاینه مربوط بسته به سن متفاوت است
در نوزادان کمتر از سه ماه، ارزیابی ثبات باسن با استفاده از مانور اورتولانی بسیار مهم است . مانور بارلو، تست Galeazzi (همچنین تست آلیس یا پرکینز نیز نامیده می شود) و تست کلیسیک نیز ممکن است مفید باشند. کاهش ابداکشن به طور کلی در این سن وجود ندارد.
بعد از سه ماهگی، ادداکشن محدود، ناهماهنگی ظاهری طول ران (در موارد یک طرفه) و آزمایش Galeazzi (برای موارد یک طرفه) و Klisic شاخص های بهتری برای DDH نسبت به بی ثباتی هستند. در سن سه ماهگی، آزمایش های بی ثباتی ارزش کمی دارند، زیرا لگن ناپایدار معمولا تثبیت شده اند (لگنی که یک بار جابجا می شود در موقعیت reduced تثبیت می شود، لگن یک بار reduced شده در موقعیت dislocated تثبیت می شود).
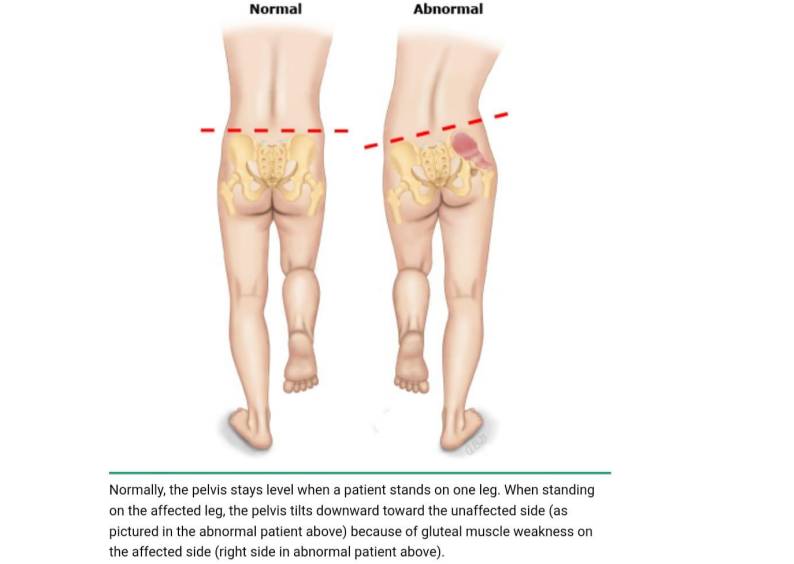
در کودکان در سن راه رفتن با DDH یک طرفه، ضعف ابدکتورهای لگن در سمت آسیب دیده ممکن است با مثبت شدن تست شیب لگن Trendelenburg (ناتوانی در حفظ لگن به صورت افقی در حالی که روی پای همان طرف ایستاده اید) و حضور ترندلنبورگ در هنگام راه رفتن نشان داده شود.
ناپایداری هیپ — هر لگن باید به صورت جداگانه از نظر کاهش پذیری و ناپایداری بررسی شود (جدول ۱) نوزاد باید روی یک سطح ثابت در وضعیت خوابیده به پشت، با لگن خمیده تا ۹۰ درجه و در چرخش خنثی باشد. معاینه باید زمانی انجام شود که نوزاد آرام است و گریه نمی کند. باسن بهتر است با برداشتن تمام لباس ها و پوشک ها از اندام تحتانی معاینه شود.
• مانور اورتولانی – ران با انگشت اشاره و وسط معاینه کننده در امتداد تروکانتر بزرگتر و شست در قسمت داخلی ران آزادانه گرفته می شود. از یک موقعیت اداکت شده، لگن به آرامی در حالی که تروکانتر را به سمت جلو بالا می برید یا فشار می آورید، ربوده می شود. از ربودن شدید باید اجتناب شود زیرا حساسیت مانور اورتولانی را کاهش می دهد. اگر مفصل ران دررفته باشد، مانور اورتولانی ممکن است آن را کاهش دهد و با یک چنگال قابل لمس همراه باشد. یک مانور مثبت Ortolani یک لگن دررفته را فرض می کند که قابل کاهش است.
• مانور بارلو – لگن به همان روشی که در مانور اورتولانی نگه داشته می شود. ران با انگشت اشاره و وسط معاینه کننده در امتداد تروکانتر بزرگتر و انگشت شست در قسمت داخلی ران آزادانه گرفته می شود. لگن به آرامی بدون اعمال فشار رو به پایین، در حالی که سر از پشت استابولوم خارج می شود، ادکتور می شود. اگر مفصل ران قابل جابجایی باشد، ممکن است حرکت خلفی و یک کل ونک قابل لمس در حین خروج سر استخوان ران از استابولوم (“تحرک خروج”) تشخیص داده شود . باسن سابله شونده با حرکت لغزشی ظریف یا احساس شلی مشخص می شود، مانند حرکت توپ تنیس در یک کاسه سوپ. یک مانور مثبت بارلو، یک لگن کاهش یافته را فرض می کند که سابلوکس یا جابجا می شود
احساس کاهش یا دررفتگی متمایز است و به بهترین وجه به عنوان “تکان” یا “کلنگ” توصیف می شود. این احساس با جهش زیاد مفصل خوش خیم، ضربه زدن یا ضربه خوردن ناشی از لق شدن تاندون ها یا رباط ها در داخل و اطراف لگن و زانو متفاوت است.
اصطلاح “هیپ کلیک” گمراه کننده است و بهتر است از آن اجتناب شود. کلیک های باسن نشان دهنده DDH نیستند.
ترکیب مانورهای بارلو و اورتولانی دارای ویژگی بالایی (تقریباً ۹۸ تا ۹۹ درصد تخمین زده می شود) در تشخیص بی ثباتی لگن هستند . حساسیت بسته به مهارت معاینه کننده، تعداد معاینات انجام شده و استاندارد تشخیصی (مانند سونوگرافی، رادیوگرافی ساده) متفاوت است. حساسیت در دست های با تجربه افزایش می یابد (از ۸۷ تا ۹۷ درصد).
عدم تقارن — یافته های معاینه نامتقارن ممکن است در DDH یک طرفه مفید باشد. با این حال، ۳۷ درصد موارد دوطرفه هستند. عدم تقارن DDH را رد نمی کند و ممکن است تشخیص را به تاخیر بیندازد.
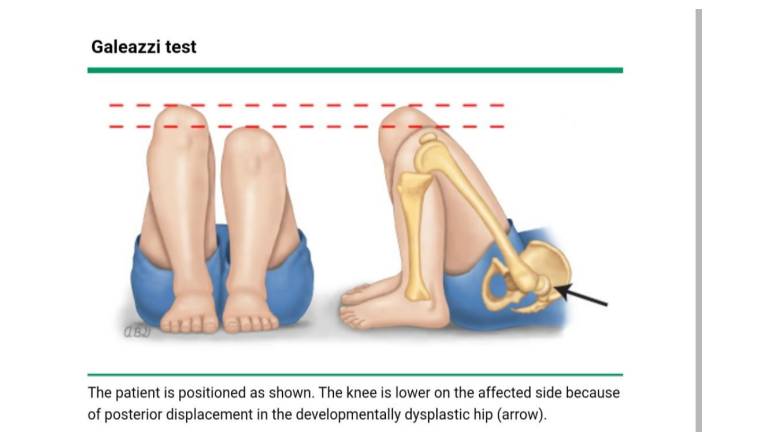
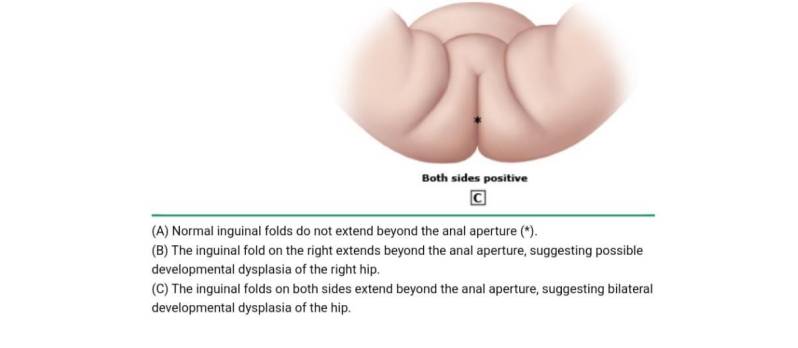
کوتاه شدن ظاهری یک استخوان ران نشانه مهمی از دررفتگی یک طرفه است و با تست Galeazzi قابل تشخیص است. این کار در حالت خوابیده به پشت، لگن خمیده تا ۹۰ درجه، زانوها خمیده و پاها صاف روی سطحی صاف و در کنار هم انجام می شود و پاشنه ها به باسن نزدیک می شوند. در این حالت، زانوها به طور معمول در یک سطح قرار دارند. در دررفتگی یک طرفه، سر استخوان ران به سمت عقب جابجا می شود و از نظر عملکردی ران را کوتاه می کند و زانوی همان طرف پایین تر از زانوی دیگر خواهد بود (شکل ۲).
تست Galeazzi مثبت برای DDH خاص نیست. سایر علل ناهماهنگی طول پا باید در نظر گرفته شوند (مانند همی هیپرتروفی، هیپوپالزی فمور، کوکسا وارا).
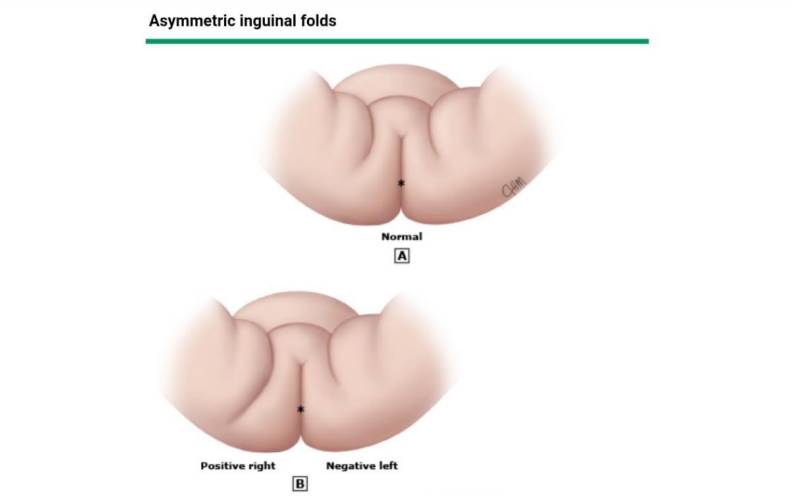
عدم تقارن در موقعیت یا تعداد چین های پوست اینگوینال، ران یا گلوتئال ممکن است سرنخی برای تشخیص DDH باشد (شکل ۳ و شکل ۴).
در مورد DDH، این افزایش چین ها به دلیل کوتاه شدن عملکردی استخوان ران با “جمع شدن” پوست و ماهیچه اطراف آن است. این یافته حساس است اما برای DDH خاص نیست، زیرا عدم تقارن چین های پوستی تقریباً در ۲۴ درصد از همه نوزادان وجود دارد. این عدم تقارن بیشتر در کودکان مبتلا به DDH یک طرفه دیده می شود.
در کودکی که در حال راه رفتن است، عدم تقارن راه رفتن ممکن است سرنخی از DDH یک طرفه ارائه دهد. راه رفتن غیرطبیعی معمولا به دلیل ناهماهنگی طول پا ایجاد می شود که منجر به تغییرات راه رفتن می شود، مانند راه رفتن با انگشت پا در سمت آسیب دیده یا خرک روی پای دیگر طرف مقابل. کودکی که دچار دررفتگی یک طرفه لگن است، در سمت آسیب دیده دچار لک ترندلنبورگ خواهد شد.
شکل ۵
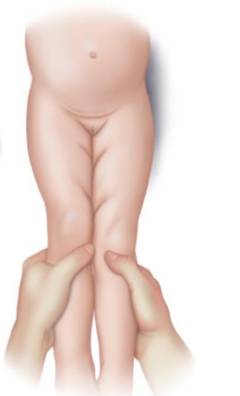
دامنه حرکت — در یک کودک بزرگتر از دو تا سه ماه، محدودیت ابداکشن (<45 درجه) قابل اطمینان ترین علامت DDH است. دامنه حرکتی نرمال در یک نوزاد به پشت خوابیده با لگن تثبیت شده برای ابداکشن بیش از ۷۵ درجه و برای اداکشن حداقل ۳۰ درجه از خط وسط است. در یک مطالعه طولی آینده نگر ۱۰ ساله که شامل ۲۸۷۶ نوزاد بود، ابداکشن محدود یک طرفه لگن پس از هشت هفتگی دارای حساسیت ۷۸ درصد و ویژگی ۹۳ درصد در تشخیص DDH تایید شده رادیوگرافی بود. در بررسی دیگری بر روی ۶۸۳ نوزاد بزرگتر از سه ماه، ابداکشن محدود یک طرفه لگن دارای حساسیت ۶۹ درصد و ویژگی ۵۴ درصد بود.
نوزادان کمتر از دو تا سه ماه ممکن است اداکشن طبیعی داشته باشند زیرا زمان کافی برای ایجاد انقباض اداکشن نداشته اند.
بیماران مبتلا به DDH یک طرفه ممکن است چرخش داخلی هیپ را افزایش دهند زیرا افزایش آنتورژن فمورال اغلب با DDH همراه است. چرخش داخلی هیپ با بیمار دراز کشیده روی میز معاینه و زانوهای خمیده ارزیابی می شود. ساق پا دور از محور بدن چرخانده می شود (چرخش داخلی لگن).
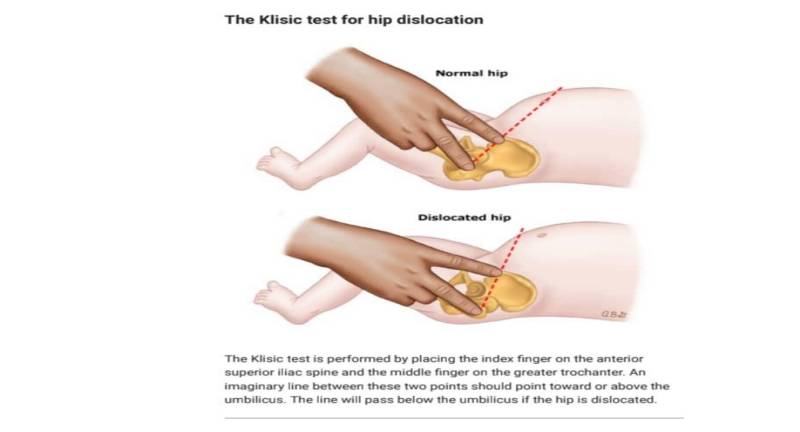
تست کلیسیک — تست کلیسیک مثبت نشان دهنده DDH است. تست کلیسیک با قرار دادن انگشت اشاره بر روی ستون فقرات ایلیاک قدامی- فوقانی و انگشت میانی روی تروکانتر بزرگ انجام می شود. یک خط فرضی بین این نقاط از ناف یا بالای ناف در یک کودک بدون DDH (تست منفی کلیسیک) می گذرد. اگر لگن دررفته باشد خط از زیر ناف عبور می کند (تست کلیسیک مثبت) زیرا تروکانتر بزرگتر در موقعیت برتر قرار دارد (شکل ۶)
تست کلیسیک ممکن است به ویژه در دررفتگی های دو طرفه مفید باشد، زمانی که ابداکشن متقارن است و علامت Galeazzi منفی است (یعنی زانوها در همان ارتفاع هستند)، زیرا نتیجه به طور مستقل برای هر طرف ارزیابی می شود و به مقایسه با طرف مقابل اندام متکی نیست.
دررفتگی دو طرفه — DDH دوطرفه در ۳۷ درصد موارد رخ می دهد. در نوزادان کمتر از سه ماه، تست های بی ثباتی (یعنی مانورهای Ortolani و Barlow) ممکن است در تشخیص DDH دو طرفه مفید باشد. با این حال، با پیشرفت DDH، دررفتگی لگن غیرقابل کاهش می شود و بی ثباتی دیگر تشخیص داده نمی شود. یافته های مربوط به تقارن (مانند علامت Galeazzi، چین های ران) در دررفتگی دو طرفه مفید نیستند.
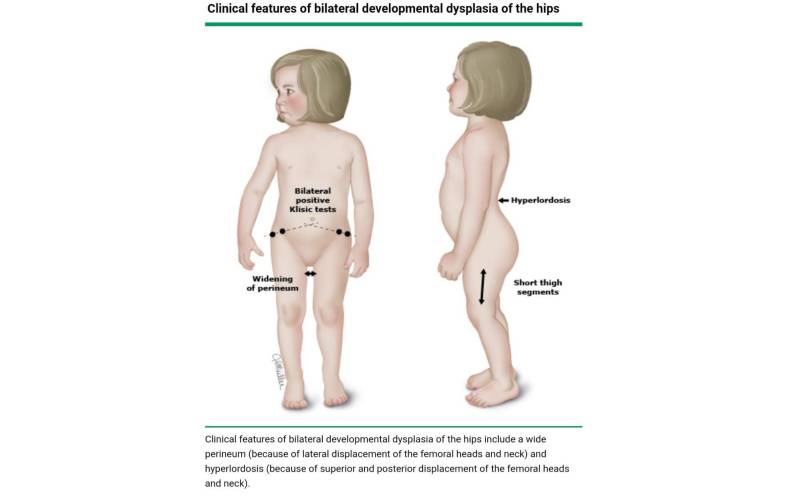
در کودکان بزرگتر از سه ماه، مهمترین یافته معاینه برای دررفتگی دو طرفه ران، ابداکشن محدود متقارن (<45 درجه) است. علائم دیگر ممکن است شامل گشاد شدن پرینه، تست های کلیسیک مثبت دو طرفه و کوتاه شدن بخش های ران نسبت به اندازه کودک باشد (شکل ۷)
هنگامی که کودک شروع به راه رفتن می کند، هایپرلوردوزیس و راه رفتن ترندلنبرگ در حال حرکت، یافته های کالسیک هستند.
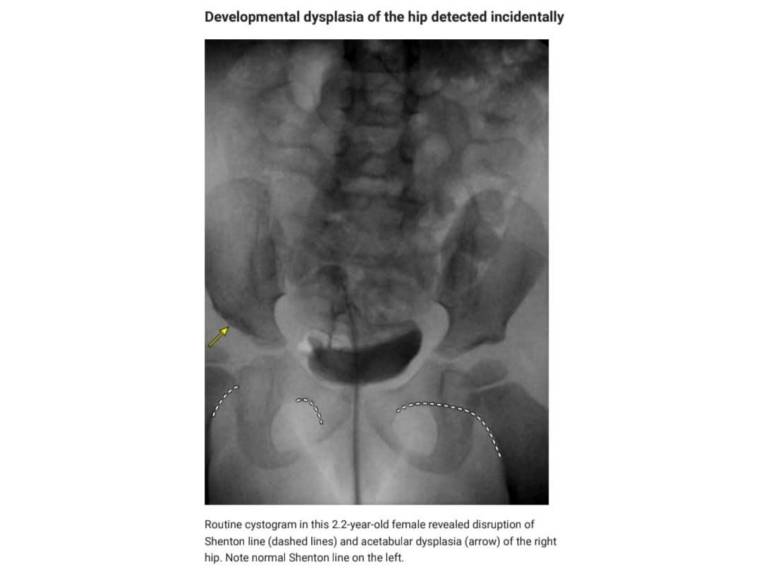
دیسپلازی بدون دررفتگی — دیسپلازی بدون دررفتگی معمولا هیچ یافته بالینی ندارد و تا نوجوانی یا اوایل بزرگسالی بدون علامت است. اغلب تنها از طریق غربالگری دقیق عوامل خطر یا به طور اتفاقی هنگامی که رادیوگرافی برای نگرانی های دیگر (به عنوان مثال، رادیوگرافی شکم برای ارزیابی انسداد روده، سیستوگرافی (تصویر ۱))
یا برای ارزیابی درد مفصل ران مربوط به فعالیت در یک نوجوان یا بالغ جوان گرفته می شود، یافت می شود.
تاریخچه طبیعی — سابقه طبیعی DDH درمان نشده به سن بیمار و شدت DDH بستگی دارد. بیشتر بی ثباتی لگن در نوزادان بلافاصله پس از تولد تثبیت می شود، زیرا شلی فیزیولوژیک کاهش می یابد و سر استخوان ران و استابولوم رشد می کنند.
در مطالعات مشاهده ای، نرخ بالایی برای رفع بی ثباتی لگن نوزاد بدون مداخله وجود دارد. در گروهی متشکل از ۱۱۹۸۹ نوزادی که توسط یک معاینه کننده معاینه شدند، ۶۰ درصد از لگن هایی که در معاینه فیزیکی در بدو تولد بی ثباتی داشتند در هفته اول زندگی تثبیت شدند و تقریباً ۹۰ درصد تا دو ماهگی تثبیت شدند. این لگن از نظر عملکردی و رادیوگرافی در سن ۱۲ ماهگی طبیعی بود. نتایج مشابهی در یک مطالعه غربالگری معمول سونوگرافی بر روی بیش از ۱۴۰۰۰ نوزاد گزارش شد: ۶ درصد بلافاصله پس از تولد دچار ناهنجاری هایی شدند که ۹۰ درصد آنها تا نه هفتگی طبیعی شدند.
نوزادان و کودکان خردسال با دررفتگی درمان نشده لگن به ندرت علائم درد یا سایر محدودیت ها را نشان می دهند. اکثر کودکان در زمان مناسب به نقاط عطف رشد می رسند. دررفتگی لگن معمولا سنی را که کودک شروع به راه رفتن می کند به تاخیر نمی اندازد. یک لگن دررفته ممکن است برای چندین سال خوب عمل کند. با این حال، ضعف در عضله ابدکتور هیپ ممکن است منجر به الگوی راه رفتن کلاسیک ترندلنبورگ شود. با گذشت زمان، ممکن است پیشرفت تدریجی ناتوانی عملکردی، درد و تسریع بیماری دژنراتیو هیپ وجود داشته باشد. خطر این عوارض به خوبی تعریف نشده است اما ممکن است با ایجاد استابولوم کاذب همراه باشد. بیماران با دررفتگی یک طرفه ممکن است ناهماهنگی طول پا، مشکلات زانو همان طرف، اسکولیوز و اختلال در راه رفتن داشته باشند. بیماران مبتلا به دررفتگی دو طرفه ممکن است دچار کمردرد شوند (شاید مربوط به افزایش لوردوز کمری باشد). هنگامی که رادیوگرافی به دلایل دیگر انجام می شود، دیسپلازی در لگن کاهش یافته یا ساب لوکس ممکن است به طور اتفاقی تشخیص داده شود. سیر بالینی بیماران با این تظاهرات متغیر است. این لگن ها اغلب در نوزادان و کودکان خردسال بدون علامت هستند و ناهنجاری های رادیوگرافی ممکن است با گذشت زمان بهبود یابد، زیرا استابولوم هنوز دارای پتانسیل بازسازی عالی است. بعد از سن مدرسه، احتمال بهبود خود به خود کم است. بیماران مبتلا به دیسپلازی مداوم بدون دررفتگی ممکن است برای مدتی بدون علامت باقی بمانند، اما ممکن است در نوجوانی یا بزرگسالی به درد مفصل ران مرتبط با فعالیت یا بیماری مفصل دژنراتیو زودرس مبتلا شوند. این در نتیجه افزایش فشار تماس غضروفی در حاشیه قدامی و جانبی استابولوم رخ می دهد. درد ممکن است بلافاصله پس از بلوغ اسکلتی، یا در زنان، در طول بارداری اول یا دوم، یا در دوران یائسگی شروع شود. بیماران ۴۰ تا ۶۰ ساله ای که با استئوآرتریت هیپ مراجعه می کنند اغلب به دیسپلازی خفیف به عنوان یک عامل کمک کننده مبتلا هستند.
تصویربرداری تشخیصی
سونوگرافی — سونوگرافی تکنیک تصویربرداری اولیه برای ارزیابی مورفولوژی و ثبات لگن نوزاد است. این یک مکمل مهم برای ارزیابی بالینی تا سن چهار تا شش ماهگی است. سونوگرافی می تواند در تایید یافته های معاینه فیزیکی و ارزیابی نوزادان با عوامل خطر که یافته های معاینه طبیعی دارند مفید باشد. اشکال عمده سونوگرافی این است که تفسیر دقیق نیاز به آموزش و تجربه دارد.
معیارهای اولتراسونوگرافی برای DDH برای تصویربرداری استاتیک (که شامل سطوح کرونال و عرضی است) و تصویربرداری پویا از لگن خم شده با و بدون مانور استرس بارلو اصلاح شده ایجاد شده است. ترکیبی از تصویربرداری استاتیک و پویا امکان ارزیابی مورفولوژی، موقعیت و ثبات لگن را فراهم می کند.
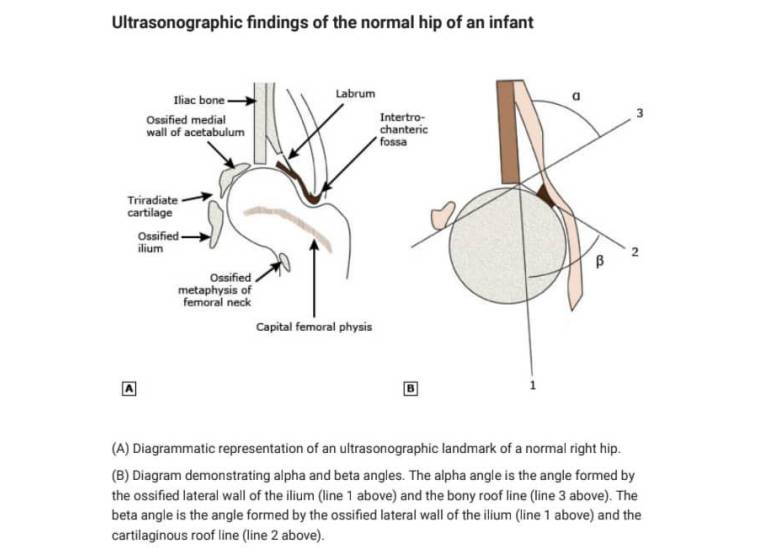
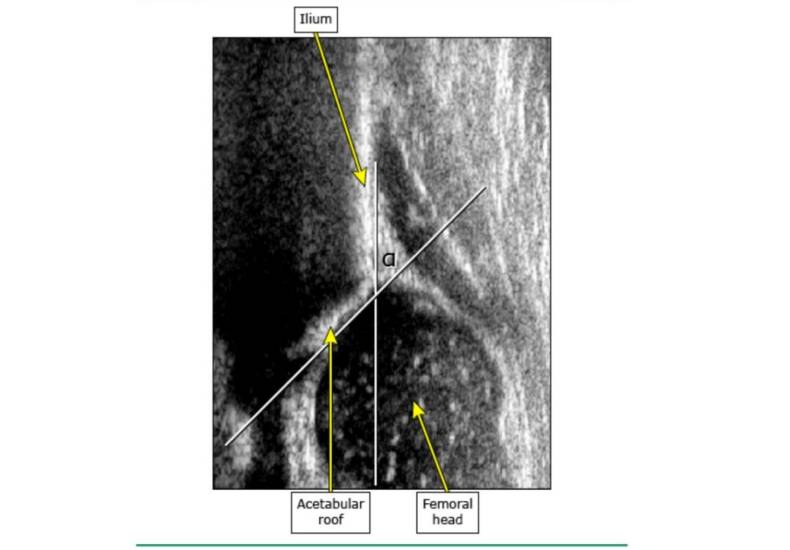
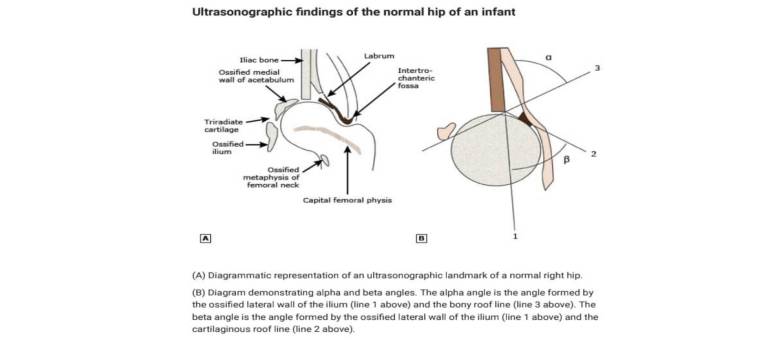
نماهای ایستا شامل یک تصویر تاجی است که نوزاد در وضعیت دکوبیتوس جانبی قرار دارد و لگن در ۳۰ تا ۴۵ درجه خم شده است. در این موقعیت، ایلیوم استخوانی شده به صورت یک خط سفید مستقیم بالای سر استخوان ران و استابولوم فوقانی مشاهده می شود (شکل ۸ و تصویر ۲)
در عمل، این تصاویر اغلب به گونه ای جهت گیری می شوند که گویی نوزاد در موقعیت جانبی دراز کشیده است، به جای اینکه در بالای سر استخوان ران به سمت چپ سر استخوان ران قرار گیرد. زاویه آلفا از دیواره جانبی ایلیوم و خط سقف استخوانی اندازه گیری می شود. زاویه بتا زاویه ای است که توسط دیواره جانبی ایلیوم و خط سقف غضروفی ایجاد می شود. این زاویه ها برای طبقه بندی DDH بر اساس سیستم Graf (شکل ۹) استفاده می شود.
پارامتر مهم دیگر درصد اپی فیز فمور است که توسط سقف استابولوم پوشانده شده است. برای نوزادان کمتر از چهار ماه، ما به طور کلی پوشش بیش از ۵۰ درصد را طبیعی می دانیم.
تکنیک پویا از تصاویر محوری و کرونال با استرس زمان واقعی سر استخوان ران، مشابه مانورهای تست بی ثباتی استفاده می کند. در چند روز اول زندگی، ۴ تا ۶ میلی متر سستی طبیعی در نظر گرفته می شود. تصویربرداری دینامیک معمولا هنگامی که لگن در طول درمان بررسی می شود حذف می شود.
رادیوگرافی ساده — رادیوگرافی ساده ممکن است در ارزیابی DDH بعد از چهار تا شش ماهگی مفید باشد. قبل از آن، رادیوگرافی ساده ارزش محدودی دارد زیرا سر استخوان ران و استابولوم غضروفی و بدون استخوان هستند. با این حال، در صورت وجود نگرانی در مورد سایر ناهنجاری های استخوانی (مانند کوکسا وارا مادرزادی، کمبود کانونی پروگزیمال فمورال و آژنزی ساکرال) ممکن است مفید باشند.
هنگامی که یک رادیوگرافی لگن در یک نوزاد تازه متولد شده درخواست می شود، باید از یک نمای قدامی – خلفی AP منفرد تشکیل شده باشد که باسن در خم شدن ۲۰ تا ۳۰ درجه باشد. نمای جانبی قورباغه غیر ضروری است و قرار گرفتن در معرض تابش را افزایش می دهد. فلکشن برای انطباق با انقباض فلکشن فیزیولوژیک لگن نوزاد ضروری است.
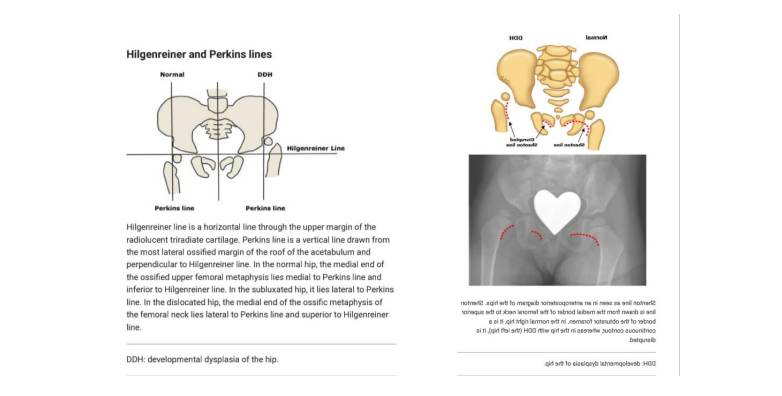
پس از چهار تا شش ماه، هنگامی که رادیوگرافی AP گرفته می شود، باسن باید در وضعیت خنثی باشد. خطوط و زوایای رادیوگرافی برای ارزیابی رشد استابولوم و موقعیت لگن استفاده می شود. یافته های رادیوگرافی ساده مطابق با DDH عبارتند از:
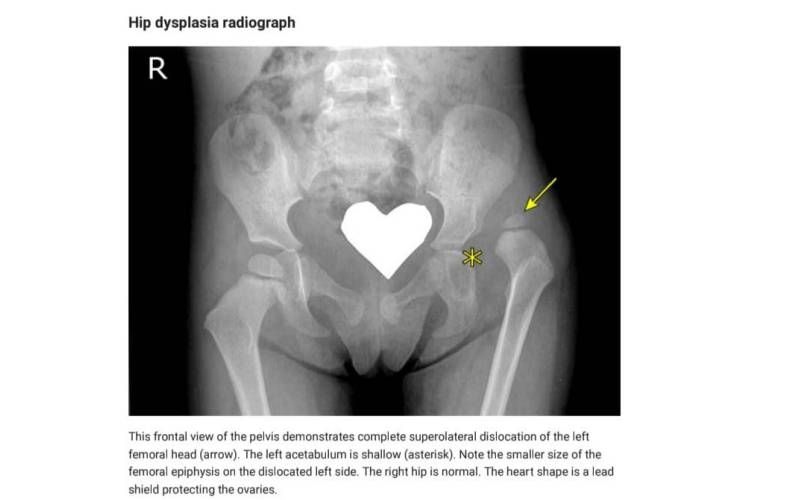
• موقعیت جانبی و فوقانی قسمت استخوانی شده سر و گردن استخوان ران (تصویر ۳ و شکل ۱۰(B-A))
• ظاهر تاخیری هسته استخوانی استخوان ران در سمت درگیر یا اندازه نامتقارن هسته استخوانی فمور.
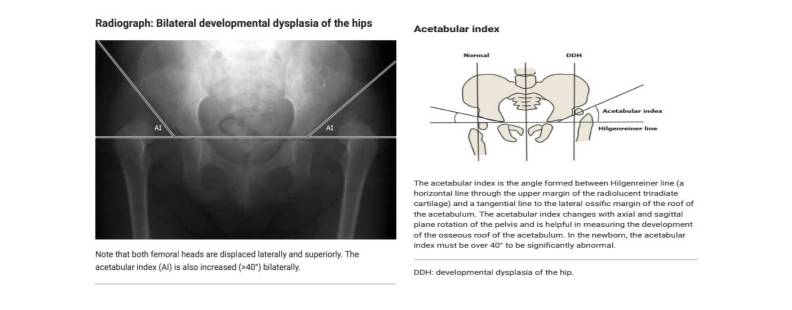
●افزایش اندیس استابولوم (شکل ۱۱ و تصویر ۴) مقادیر طبیعی برای شاخص استابولوم به شرح زیر است: <35 درجه در هنگام تولد. کمتر از ۲۵ درجه در ۱ سال؛ کمتر از ۲۰ درجه در ۲ تا ۳ سال؛ کمتر از ۱۵ درجه در ۶ تا ۷ سال؛ کمتر از ۱۱ تا ۱۲ درجه در ۱۰ سال؛ و کمتر از ۱۰ درجه در ۱۵ سال.
سایر روش های تصویربرداری، مانند آرتروگرافی، توموگرافی کامپیوتری (CT) و تصویربرداری رزونانس مغناطیسی (MRI) در تشخیص DDH مفید نیستند، اما ممکن است برای ارزیابی کاهش پس از جراحی استفاده شوند. آرتروگرافی)تزریق کنتراست رادیواپک به مفصل ران) و تصویربرداری سه بعدی، مانند MRI یا CT، اغلب برای تایید کاهش موفقیت آمیز و تعیین موقعیت سر استخوان ران در داخل استابولوم پس از گچ گیری انجام می شود. پروتکل های اطفال که شامل دوزهای کاهش یافته تابش است باید استفاده شود.
MRI به طور معمول در ارزیابی تشخیصی کودک خردسال مبتلا به DDH استفاده نمی شود، اما استفاده از آن در ارزیابی کاهش پس از جراحی رایج تر می شود. در مقایسه با MRI ،CT بیمار را در معرض هیچ اشعه قرار نمی دهد و اطلاعاتی در مورد عروق سر استخوان ران ارائه می دهد. همچنین برای ارزیابی عواقب طولانی مدت DDH نیمه درمان شده یا درمان نشده، مانند پارگی لب و آرتریت مفید است.
تشخیص
تشخیص DDH در نوزادان معمولا با معاینه فیزیکی که نشان د هنده بی ثباتی لگن است (جدول ۱). عدم تقارن (در موارد یک طرفه) و یا ابداکشن محدود انجام می شود. یافته های معاینه DDH با توجه به سن متفاوت است (جدول ۲).
تصویربرداری تشخیصی را می توان برای تشخیص در نوزادانی با یافته های معاینه غیرقطعی استفاده کرد. تصویربرداری تشخیصی همچنین ممکن است برای تشخیص در نوزادانی که فاکتورهای خطر و معاینه طبیعی دارند استفاده شود.
سونوگرافی به طور کلی برای نوزادان کمتر از چهار تا شش ماه و رادیوگرافی ساده برای نوزادان بزرگتر از چهار تا شش ماه ترجیح داده می شود. اندازه گیری های سونوگرافی (شکل ۸).
برای طبقه بندی DDH بر اساس سیستم گراف استفاده می شود. یافته های رادیوگرافی ساده DDH شامل موقعیت جانبی و فوقانی قسمت استخوانی شده سر و گردن، افزایش شاخص استابولوم و تاخیر در ظاهر شدن هسته استخوانی استخوان ران در سمت درگیر یا اندازه های نامتقارن هسته های استخوانی فمور است.
رویکرد به تشخیص و ارجاع
رویکرد ما برای تشخیص و ارجاع برای DDH با یافته های معاینه بالینی، سن نوزاد و عوامل خطر متفاوت است. به طور کلی با دستورالعمل عمل بالینی آکادمی جراحان ارتوپدی آمریکا (AAOS) برای تشخیص و مدیریت غیرجراحی، DDH دستورالعمل عمل بالینی آکادمی اطفال آمریکا (AAP) برای تشخیص زودهنگام DDH مطابقت دارد. معیارهای تناسب کالج آمریکایی رادیولوژی (ACR) برای، DDH و راهنمای موسسه سونوگرافی آمریکا در پزشکی برای تشخیص و ارزیابی. DDH اعمال و ترجیحات محلی جراحان ارتوپد ممکن است متفاوت باشد، به ویژه در خارج از ایالات متحده.
اورتولانی مثبت یا ابداکشن محدود/نامتقارن — برای نوزادان (در هر سنی) با مانور اورتولانی مثبت (یعنی دررفتگی لگن) یا ابداکشن محدود یا نامتقارن (یعنی دررفتگی لگن غیرقابل تقلیل) پیشنهاد می کنیم به یک جراح ارتوپد ارجاع دهید. در تشخیص و درمان DDH برای ارزیابی و مدیریت بیشتر تجربه دارد. تصمیم گیری در مورد مطالعات تصویربرداری را می توان به مشاور موکول کرد که ممکن است در طول مدیریت و پیگیری از مطالعات مختلفی استفاده کند.
بارلو مثبت — برای نوزادان (در هر سنی) با مانور بارلو مثبت (یعنی لگن قابل جابجایی یا سابلوکساسیون)، ما نظارت بر لگن (یعنی معاینات پیگیری سریال) را پیشنهاد می کنیم تا از ایجاد ثبات لگن اطمینان حاصل شود. نظارت بر لگن ممکن است توسط پزشک مراقبت های اولیه یا جراح ارتوپدی که در تشخیص و مدیریت DDH با توجه به تمرین و ترجیح محلی با تجربه است، انجام شود.
بررسی غیربهینه یا غیرقطعی
●نوزاد – اگر معاینه نوزاد نابهینه باشد (به عنوان مثال، نوزاد به اندازه کافی آرام نیست تا یک ارزیابی قابل اعتماد از حرکت و ثبات داشته باشد) یا بی نتیجه باشد (به عنوان مثال، شواهدی از بی ثباتی وجود ندارد، اما با کلیک های مفصلی یا عدم تقارن ران)، نوزاد مجدداً انجام می شود. – در ویزیت بعدی نظارت بهداشتی (معمولا در سن دو تا چهار هفتگی) معاینه شود.
●دو تا چهار هفته – برای نوزادان دو تا چهار هفته ای با معاینه بی نتیجه (مثلا شواهدی از بی ثباتی وجود ندارد، اما با کلیک های مفصلی یا عدم تقارن ران (پیشنهاد می کنیم به یک جراح ارتوپد با تجربه در تشخیص و تشخیص ارجاع دهید. درمان DDH برای ارزیابی و مدیریت بیشتر روش های جایگزین، بسته به سطح سوء ظن، شامل:
• سونوگرافی در شش تا هشت هفته (تعدیل شده برای نارسی)، در این مرحله، ناهنجاری های سونوگرافی “کوچک” که در نوزادان یافت می شود باید برطرف شود
• پیگیری بالینی باید ادامه داشته باشد.
چهار هفته به بالا – برای نوزادان چهار هفته و بالاتر با یافته های ظریف یا غیر اختصاصی، تصویربرداری را پیشنهاد می کنیم. اگر نوزاد کمتر از شش ماه باشد سونوگرافی انجام می دهیم و اگر شیرخوار بزرگتر از شش ماه باشد رادیوگرافی ساده انجام می دهیم.
معاینه طبیعی و عوامل خطر — تصمیمات مربوط به تصویربرداری از نوزادان با معاینه فیزیکی طبیعی و عوامل خطر برای DDH بهتر است بر اساس مورد به مورد گرفته شود. اگر معاینه نوزاد طبیعی باشد، خطر دررفتگی تا حد زیادی کاهش می یابد.
ما تصویربرداری (با سونوگرافی در سن چهار تا شش هفتگی {تعدیل شده برای نارس}) را برای نوزادان با هر یک از عوامل خطر زیر دریافت می کنیم:
●نوزادان دختر و پسر با موقعیت بریچ در هفته ۳۴ حاملگی ≤ (خواه نسخه خارجی سفالیک موفقیت آمیز بوده یا لازم بوده باشد)
●سابقه خانوادگی DDH (از جمله تعویض مفصل ران برای دیسپلازی قبل از ۴۰ سالگی در یکی از بستگان نزدیک)
●سابقه بی ثباتی بالینی در معاینه
اگر سونوگرافی در دسترس نباشد یا کودکی با یک عامل خطر در شش ماهگی یا بیشتر مراجعه کند، غربالگری ممکن است با رادیوگرافی ساده از لگن و پلویس انجام شود.
باسن نوزادانی که فاکتورهای خطر DDH دارند و در شش هفته (سونوگرافی) یا چهار ماهگی (رادیوگرافی ساده) معاینه طبیعی و مطالعات تصویربرداری طبیعی دارند، باید در بازدیدهای بعدی نظارت بهداشتی تا زمانی که کودک به طور مستقل راه برود بررسی شود. یافته های معاینه مربوطه بسته به سن متفاوت است.
تشخیص افتراقی – ملاحظات عمده در تشخیص افتراقی DDH در نوزادان شامل سایر علل ناهماهنگی طول پا در نوزادان با تست Galeazzi مثبت است، مانند:
- نقص فوکال پروگزیمال فمور، یک بیماری مادرزادی غیرشایع با طیفی است که از هیپوپلازی سر استخوان ران تا عدم وجود مادرزادی همه به جز اپیفیز دیستال فمورال متغیر است.
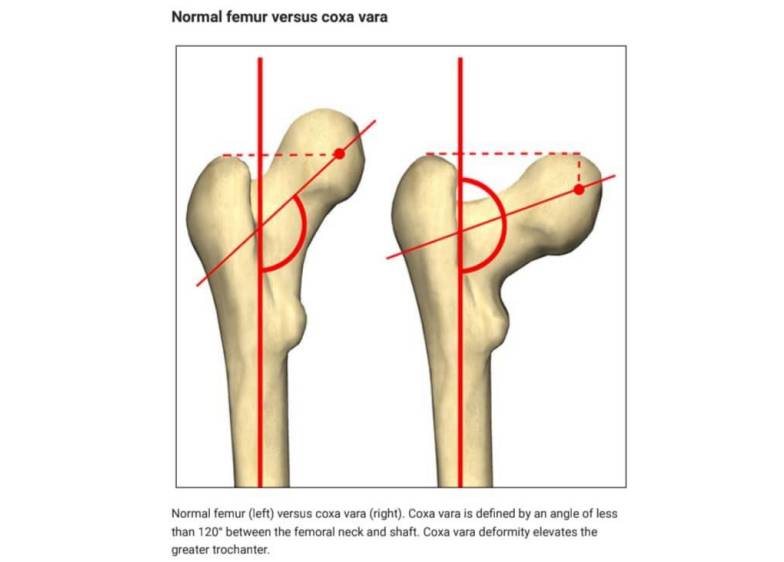
- کوکسا وارا، با زاویه کمتر از ۱۲۰ درجه بین گردن فمور و شفت، که منجر به بالا رفتن تروکانتر بزرگتر می شود (شکل ۱۲) تعریف می شود.
- همی هیپرتروفی یا همی هیپرپلازی (به عنوان مثال، سندرم بکویث ویدمن)
- آژنزیس ساکرال با تغییر شکل اندام
غربالگری برای DDH — توصیه هایی برای غربالگری نوزادان تازه متولد شده از نظر DDH از کشوری به کشور دیگر متفاوت است. برخی از کشورها غربالگری همه نوزادان را توصیه می کنند، در حالی که برخی دیگر غربالگری را فقط برای کسانی که عوامل خطر انتخابی دارند توصیه می کنند. سنی که کودک در آن غربالگری می شود و رویکرد غربالگری (مثلا معاینه بالینی در مقابل سونوگرافی در مقابل رویکرد مبتنی بر طبقه بندی خطر) نیز از کشوری به کشور دیگر متفاوت است.
راهنمای عمل بالینی آکادمی جراحان ارتوپدی آمریکا در سال ۲۰۱۴، غربالگری جهانی اولتراسوند نوزادان را برای DDH توصیه می کند. کارگروه خدمات پیشگیرانه ایالات متحده به این نتیجه رسید که شواهد برای توصیه غربالگری معمول نوزادان برای DDH به عنوان وسیله ای برای جلوگیری از پیامدهای نامطلوب کافی نیست و غربالگری نوزاد منجر به تشخیص بیش از حد لگن می شود که سودی ندارد و ممکن است با درمان آسیب ببیند. انجمن ارتوپدی اطفال آمریکای شمالی (POSNA) کمبود داده برای حمایت از غربالگری را تصدیق می کند، اما به ارزش تشخیص زود هنگام در پیشگیری از عوارض طولانی مدت اشاره می کند. POSNA توصیه می کند که دستورالعمل های عمل بالینی آکادمی اطفال آمریکا را همراه با ارزیابی بالینی برای DDH در بدو تولد و هر ویزیت کودک خوب تا زمانی که کودک به طور طبیعی راه میرود و تصویربرداری انتخابی از نوزادان با عوامل خطر را دنبال کنید. این رویکرد توسط یک تجزیه و تحلیل تصمیم پشتیبانی می شود که غربالگری همه نوزادان با معاینه فیزیکی را توصیه می کند.
درمان مشکلات رشدی لگن
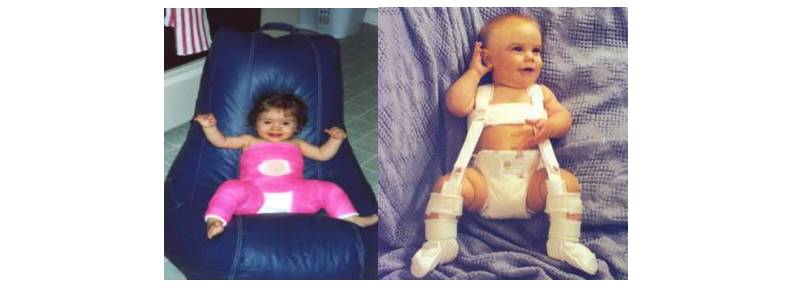
مهار پاولیک نوزادانی که در اوایل زندگی مبتلا به DDH تشخیص داده می شوند معمولا با یک آتل پارچه ای به نام مهار پاولیک درمان می شوند. این کار هر دو باسن کودک شما را در یک موقعیت ثابت نگه می دارد و به آنها اجازه می دهد تا به طور طبیعی رشد کنند.
این هارنس باید به مدت چندین هفته به طور مداوم پوشیده شود و نباید توسط کسی به جز یک متخصص بهداشت برداشته شود. مهار ممکن است در طول قرارهای بعدی تنظیم شود.
در نهایت، ممکن است در مورد برداشتن و تعویض هارنس برای مدت کوتاهی توصیه شود تا زمانی که بتوان آن را برای همیشه جدا کرد. شما تشویق خواهید شد که به کودک خود اجازه دهید آزادانه در زمانی که بند خاموش است حرکت کند. شنا اغلب توصیه می شود.
اگر کودک پس از ۶ ماهگی با DDH تشخیص داده شود، یا اگر هارنس پاولیک کمکی نکرده باشد، ممکن است جراحی لازم باشد.
این شامل قرار دادن سر استخوان ران در حفره لگن است.
جراحی کاهش تحت بیهوشی عمومی انجام می شود و ممکن است به صورت زیر انجام شود:
جااندازی بسته – سر استخوان ران بدون ایجاد برش بزرگ در حفره مفصل ران قرار می گیرد.
جااندازی باز – برشی در کشاله ران ایجاد می شود تا جراح بتواند سر استخوان ران را در حفره لگن قرار دهد.
ممکن است کودک حداقل ۱۲ هفته پس از عمل نیاز به گچ گرفتن داشته باشد. لگن آنها پس از ۶ هفته مجدداً تحت بیهوشی عمومی بررسی می شود تا از پایداری و بهبودی آن اطمینان حاصل شود. پس از این بررسی، کودک احتمالا حداقل ۶ هفته دیگر گچ می گیرد تا لگن او به طور کامل تثبیت شود.
برخی از کودکان همچنین ممکن است به جراحی استخوان (استئوتومی) در حین جااندازی باز یا در تاریخ بعدی برای اصالح هرگونه ناهنجاری استخوانی نیاز داشته باشند.
Weinstein SL, Mubarak SJ, Wenger DR. Developmental hip dysplasia and dislocation: Part II. Instr .1
Course Lect 2004; 53:531.
Shaw BA, Segal LS, SECTION ON ORTHOPAEDICS. Evaluation and Referral for .2
Developmental Dysplasia of the Hip in Infants. Pediatrics 2016; 138.
Lambeek AF, De Hundt M, Vlemmix F, et al. Risk of developmental dysplasia of the hip in breech .3
presentation: the effect of successful external cephalic version. BJOG 2013; 120:607.
American Academy of Orthopaedic Surgeons. Detection and nonoperative management of pediatr .4
ic developmental dysplasia of the hip in infants up to six months of age. Evidence-based clinical p
ractice guideline. September 2014. http://www.aaos.org/research/guidelines/DDHGuidelineFINA
L.pdf.
Schwend RM, Schoenecker P, Richards BS, et al. Screening the newborn for developmental .5
dysplasia of the hip: now what do we do? J Pediatr Orthop 2007; 27:607.
Patel H, Canadian Task Force on Preventive Health Care. Preventive health care, 2001 update: .6
screening and management of developmental dysplasia of the hip in newborns. CMAJ 2001;
۱۶۴:۱۶۶۹٫
BARLOW TG. EARLY DIAGNOSIS AND TREATMENT OF CONGENITAL DISLOCATION .7
OF THE HIP. Proc R Soc Med 1963; 56:804.
Ortolani M. Congenital hip dysplasia in the light of early and very early diagnosis. Clin Orthop .8
Relat Res 1976; :6.
COLEMAN SS. Diagnosis of congenital dysplasia of the hip in the newborn infant. J Am Med .9
Assoc 1956; 162:548.
Bond CD, Hennrikus WL, DellaMaggiore ED. Prospective evaluation of newborn soft-tissue hip .10
“clicks” with ultrasound. J Pediatr Orthop 1997; 17:199.
Kane TP, Harvey JR, Richards RH, et al. Radiological outcome of innocent infant hip clicks. J .11
Pediatr Orthop B 2003; 12:259.
Nie K, Rymaruk S, Paton RW. Clicky hip alone is not a true risk factor for developmental dysplasia .12
of the hip. Bone Joint J 2017; 99-B:1533.
Dezateux C, Brown J, Arthur R, et al. Performance, treatment pathways, and effects of alternative .13
policy options for screening for developmental dysplasia of the hip in the United Kingdom. Arch
Dis Child 2003; 88:753.
Baronciani D, Atti G, Andiloro F, et al. Screening for developmental dysplasia of the hip: from .14
theory to practice. Collaborative Group DDH Project. Pediatrics 1997; 99:E5.
Poul J, Bajerova J, Sommernitz M, et al. Early diagnosis of congenital dislocation of the hip. J .15
Bone Joint Surg Br 1992; 74:695.
Fulton MJ, Barer ML. Screening for congenital dislocation of the hip: an economic appraisal. Can .16
Med Assoc J 1984; 130:1149.
Burger BJ, Burger JD, Bos CF, et al. Neonatal screening and staggered early treatment for .17
congenital dislocation or dysplasia of the hip. Lancet 1990; 336:1549.
Groarke PJ, McLoughlin L, Whitla L, et al. Retrospective Multicenter Analysis of the Accuracy of .18
Clinical Examination by Community Physicians in Diagnosing Developmental Dysplasia of the
Hip. J Pediatr 2017; 181:163.
Dunn PM. Perinatal observations on the etiology of congenital dislocation of the hip. Clin Orthop .19
Relat Res 1976; :11.
Anderton MJ, Hastie GR, Paton RW. The positive predictive value of asymmetrical skin creases in .20
the diagnosis of pathological developmental dysplasia of the hip. Bone Joint J 2018; 100-B:675.
Ando M, Gotoh E. Significance of inguinal folds for diagnosis of congenital dislocation of the hip .21
in infants aged three to four months. J Pediatr Orthop 1990; 10:331.
Screening for the detection of congenital dislocation of the hip. Arch Dis Child 1986; 61:921. .22
Novacheck TF. Developmental dysplasia of the hip. Pediatr Clin North Am 1996; 43:829. .23
Choudry Q, Goyal R, Paton RW. Is limitation of hip abduction a useful clinical sign in the diagnosis .24
of developmental dysplasia of the hip? Arch Dis Child 2013; 98:862.
Castelein RM, Korte J. Limited hip abduction in the infant. J Pediatr Orthop 2001; 21:668. .25
Sankar WN, Neubuerger CO, Moseley CF. Femoral anteversion in developmental dysplasia of the .26
hip. J Pediatr Orthop 2009; 29:885.
Loder RT, Skopelja EN. The epidemiology and demographics of hip dysplasia. ISRN Orthop 2011; .27
۲۰۱۱:۲۳۸۶۰۷٫
Wedge JH, Wasylenko MJ. The natural history of congenital dislocation of the hip: a critical .28
review. Clin Orthop Relat Res 1978; :154.
Wedge JH, Wasylenko MJ. The natural history of congenital disease of the hip. J Bone Joint Surg .29
Br 1979; 61-B:334.
Weinstein SL. Natural history of congenital hip dislocation (CDH) and hip dysplasia. Clin Orthop .30
Relat Res 1987; :62.
Crawford AH, Mehlman CT, Slovek RW. The fate of untreated developmental dislocation of the .31
hip: long-term follow-up of eleven patients. J Pediatr Orthop 1999; 19:641.
Bialik V, Bialik GM, Blazer S, et al. Developmental dysplasia of the hip: a new approach to .32
incidence. Pediatrics 1999; 103:93.
Castelein RM, Sauter AJ. Ultrasound screening for congenital dysplasia of the hip in newborns: its .33
value. J Pediatr Orthop 1988; 8:666.
Terjesen T, Holen KJ, Tegnander A. Hip abnormalities detected by ultrasound in clinically normal .34
newborn infants. J Bone Joint Surg Br 1996; 78:636.
Marks DS, Clegg J, al-Chalabi AN. Routine ultrasound screening for neonatal hip instability. Can .35
it abolish late-presenting congenital dislocation of the hip? J Bone Joint Surg Br 1994; 76:534.
Dezateux C, Rosendahl K. Developmental dysplasia of the hip. Lancet 2007; 369:1541. .36
Harris NH, Lloyd-Roberts GC, Gallien R. Acetabular development in congenital dislocation of the .37
hip. With special reference to the indications for acetabuloplasty and pelvic or femoral realignment
osteotomy. J Bone Joint Surg Br 1975; 57:46.
Schwend RM, Pratt WB, Fultz J. Untreated acetabular dysplasia of the hip in the Navajo. A 34 year .38
case series followup. Clin Orthop Relat Res 1999; :108.
Wood MK, Conboy V, Benson MK. Does early treatment by abduction splintage improve the .39
development of dysplastic but stable neonatal hips? J Pediatr Orthop 2000; 20:302.
Lehmann HP, Hinton R, Morello P, Santoli J. Developmental dysplasia of the hip practice .40
guideline: technical report. Committee on Quality Improvement, and Subcommittee on
Developmental Dysplasia of the Hip. Pediatrics 2000; 105:E57.
Elbourne D, Dezateux C, Arthur R, et al. Ultrasonography in the diagnosis and management of .41
developmental hip dysplasia (UK Hip Trial): clinical and economic results of a multicentre
randomised controlled trial. Lancet 2002; 360:2009.
Expert Panel on Pediatric Imaging:, Nguyen JC, Dorfman SR, et al. ACR Appropriateness .42
Criteria® Developmental Dysplasia of the Hip-Child. J Am Coll Radiol 2019; 16:S94.
Dias JJ, Thomas IH, Lamont AC, et al. The reliability of ultrasonographic assessment of neonatal .43
hips. J Bone Joint Surg Br 1993; 75:479.
AIUM-ACR-SPR-SRU Practice Parameter for the Performance of an Ultrasound Examination for .44
Detection and Assessment of Developmental Dysplasia of the Hip. J Ultrasound Med 2018; 37:E1.
Graf R. New possibilities for the diagnosis of congenital hip joint dislocation by ultrasonography. .45
J Pediatr Orthop 1983; 3:354.
Harcke HT, Pruszczynski B. Hip ultrasound for developmental dysplasia: the 50% rule. Pediatr .46
Radiol 2017; 47:817.
Quader N, Schaeffer EK, Hodgson AJ, et al. A Systematic Review and Meta-analysis on the .47
Reproducibility of Ultrasound-based Metrics for Assessing Developmental Dysplasia of the Hip. J
Pediatr Orthop 2018; 38:e305.
Harcke HT, Grissom LE. Performing dynamic sonography of the infant hip. AJR Am J Roentgenol .48
۱۹۹۰; ۱۵۵:۸۳۷٫
Hensinger RN. Standards in Pediatric Orthopedics: Tables, Charts, and Graphs Illustrating Growt .49
h, Lippincott Williams & Wilkins, Philadelphia 1986. p.68.
Desai AA, Martus JE, Schoenecker J, Kan JH. Spica MRI after closed reduction for developmental .50
dysplasia of the hip. Pediatr Radiol 2011; 41:525.
Jaramillo D, Villegas-Medina O, Laor T, et al. Gadolinium-enhanced MR imaging of pediatric .51
patients after reduction of dysplastic hips: assessment of femoral head position, factors impeding
reduction, and femoral head ischemia. AJR Am J Roentgenol 1998; 170:1633.
Mulpuri K, Song KM, Gross RH, et al. The American Academy of Orthopaedic Surgeons .52
Evidence-Based Guideline on Detection and Nonoperative Management of Pediatric
Developmental Dysplasia of the Hip in Infants up to Six Months of Age. J Bone Joint Surg Am
۲۰۱۵; ۹۷:۱۷۱۷٫
Pacana MJ, Hennrikus WL, Slough J, Curtin W. Ultrasound Examination for Infants Born Breech .53
by Elective Cesarean Section With a Normal Hip Exam for Instability. J Pediatr Orthop 2017;
۳۷:e15.
Reidy M, Collins C, MacLean JGB, Campbell D. Examining the effectiveness of examination at .54
۶-۸ weeks for developmental dysplasia: testing the safety net. Arch Dis Child 2019; 104:953.
Morris AR, Thomas JMC, Reading IC, Clarke NMP. Does Late Hip Dysplasia Occur After Normal .55
Ultrasound Screening in Breech Babies? J Pediatr Orthop 2019; 39:187.
Imrie M, Scott V, Stearns P, et al. Is ultrasound screening for DDH in babies born breech sufficient? .56
J Child Orthop 2010; 4:3.
Godley DR. Assessment, diagnosis, and treatment of developmental dysplasia of the hip. JAAPA .57
۲۰۱۳; ۲۶:۵۴٫
Shipman SA, Helfand M, Moyer VA, Yawn BP. Screening for developmental dysplasia of the hip: .58
a systematic literature review for the US Preventive Services Task Force. Pediatrics 2006;
۱۱۷:e557.
Broadhurst C, Rhodes AML, Harper P, et al. What is the incidence of late detection of .59
developmental dysplasia of the hip in England?: a 26-year national study of children diagnosed
after the age of one. Bone Joint J 2019; 101-B:281.
Mahan ST, Katz JN, Kim YJ. To screen or not to screen? A decision analysis of the utility of .60
screening for developmental dysplasia of the hip. J Bone Joint Surg Am 2009; 91:1705.
McAbee GN, Donn SM, Mendelson RA, et al. Medical diagnoses commonly associated with .61
pediatric malpractice lawsuits in the United States. Pediatrics 2008; 122:e1282.
United States Preventive Services Task Force. Developmental hip dysplasia: Screening. Available .62
at: https://www.uspreventiveservicestaskforce.org/BrowseRec/InactiveTopic/224 (Accessed on O
ctober 15, 2018)..












دیدگاه خود را ثبت کنید
Want to join the discussion?Feel free to contribute!